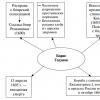
Poäng för kemiprov. Struktur för CMM i kemi
Federal Service for Supervision in Education and Science
(Rosobrnadzor)
27/02/2019
nr 10-151 Federal service för tillsyn inom utbildnings- och vetenskapsområdet i enlighet med punkt 21 i förfarandet för genomförande av statlig slutlig certifiering för utbildningsprogram för grundläggande allmän utbildning, godkänd genom order från utbildningsministeriet i Ryssland och Rosobrnadzor daterad den 7 november 2018 nr 189 /1513 (registrerad av Rysslands justitieministerium den 10 december 2018, registreringsnummer 52953) (hädanefter - förfarandet), skickar rekommendationer för användning i arbetet med att fastställa det minsta antalet primärpoäng som bekräftar att eleverna har behärskat utbildningsprogram grundläggande allmän utbildning i enlighet med kraven i den federala statliga utbildningsstandarden för grundläggande allmän utbildning (nedan - minsta kvantitet primärpoäng), rekommendationer för omvandling av summan av primärpoäng för tentamensuppgifter för huvudprovet (nedan - OGE) och det statliga slutprovet (nedan - GVE).
in i ett fempunktsbedömningssystem 2019 I enlighet med punkt 22 i förfarandet, verkställande myndigheter för subjekten ryska federationen
, utföra offentlig förvaltning inom utbildningsområdet, säkerställa genomförandet av statlig slutlig certifiering för utbildningsprogram för grundläggande allmän utbildning, inklusive fastställande av det minsta antalet primära poäng, och även säkerställa överföringen av summan av primärpoäng för tentamensuppgifter av OGE och GVE till ett fempunktsbedömningssystem. Användning: för 14 l.
Biträdande chef: A.A. Muzaev Skala för omräkning av den primära poängen för slutförande tentamen
till ett betyg på en femgradig skala.
2019 Kemi.
år.
Det maximala antalet poäng som en OGE-deltagare kan få för att genomföra hela examinationsarbetet (utan ett riktigt experiment) är 34 poäng.
0-8 poäng - markera "2"
9-17 poäng - markera "3"
18-26 poäng - markera "4"
Tentamensresultaten kan användas vid antagning av elever till specialiserade klasser för utbildning i gymnasieutbildningar.
Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
Det maximala antalet poäng som en OGE-deltagare kan få för att genomföra hela examinationsarbetet (utan ett riktigt experiment) är 34 poäng.
Det maximala antalet poäng som en deltagare i OGE kan få för att genomföra hela examinationsarbetet (med ett riktigt experiment) är 38 poäng.
9-18 poäng - markera "3"
19-28 poäng - markera "4"
29-38 poäng - markera "5"
Tentamensresultaten kan användas vid antagning av elever till specialiserade klasser för utbildning i gymnasieutbildningar. Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 25 poäng.
2018
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
18-26 poäng - markera "4"
27-34 poäng - markera "5"
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (att arbeta med ett riktigt experiment, demoversion 2)
9-18 poäng - markera "3"
19-28 poäng - markera "4"
29-38 poäng - markera "5"
2018
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
18-26 poäng - markera "4"
2017
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (att arbeta med ett riktigt experiment, demoversion 2)
9-18 poäng - markera "3"
Det maximala antalet poäng som en examinand kan få för att fullgöra hela tentamensuppsatsen (utan själva experimentet) är 34 poäng.
Det maximala antalet poäng som en examinand kan få för att fullfölja hela tentamensuppsatsen (med ett riktigt experiment) är 38 poäng.
29-38 poäng - markera "5"
2018
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
18-26 poäng - markera "4"
27-34 poäng - markera "5"
2017
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (att arbeta med ett riktigt experiment, demoversion 2)
9-18 poäng - markera "3"
Det maximala antalet poäng som en examinand kan få för att fullgöra hela tentamensuppsatsen (utan själva experimentet) är 34 poäng.
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor. En riktlinje för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 25 poäng.
29-38 poäng - markera "5"
2018
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
18-26 poäng - markera "4"
2016
2017
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (att arbeta med ett riktigt experiment, demoversion 2)
9-18 poäng - markera "3"
Det maximala antalet poäng som en examinand kan få för att fullgöra hela tentamensuppsatsen (utan själva experimentet) är 34 poäng.
2015
29-38 poäng - markera "5"
2018
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
18-26 poäng - markera "4"
2016
2017
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (att arbeta med ett riktigt experiment, demoversion 2)
9-18 poäng - markera "3"
Det maximala antalet poäng som en examinand kan få för att fullgöra hela tentamensuppsatsen (utan själva experimentet) är 34 poäng.
Det rekommenderas att markera "5" om den utexaminerade av de totala poängen som är tillräckliga för att erhålla detta betyg fick 5 eller fler poäng för att slutföra uppgifterna i del 3. Provresultaten kan användas vid antagning av studenter till specialiserade klasser på gymnasiet skola.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
27-33 poäng - markera "5"
Det rekommenderas att ge betyget "5" om den utexaminerade utexaminerade fick 5 eller fler poäng av det totala antalet poäng som är tillräckligt för att erhålla detta betyg för att utföra uppgifterna i del 3.
2012
Det maximala antalet poäng som en examinand kan få för att fullgöra hela examinationsarbetet är 33 poäng.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
27-33 poäng - markera "5"
Det rekommenderas att ge betyget "5" om den utexaminerade utexaminerade fick 5 eller fler poäng av det totala antalet poäng som är tillräckligt för att erhålla detta betyg för att utföra uppgifterna i del 3.
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor. Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
2011
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (arbete utan ett riktigt experiment, demoversion 1)
0-8 poäng - markera "2"
9-17 poäng - markera "3"
27-33 poäng - markera "5"
Den föreslagna nedre poänggränsen för att markera "3" är en riktlinje för territoriella ämnesuppdrag och kan sänkas, men inte lägre än till 6 poäng.
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor. Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
2010
0-10 poäng - markera "2"
11-19 poäng - markera "3"
20-28 poäng - markera "4"
29-34 poäng - markera "5"
2009
0-10 poäng - markera "2"
11-18 poäng - markera "3"
19-27 poäng - markera "4"
28-33 poäng - markera "5"
Kommunal budgetutbildningsanstalt
“Grundskola nr 4, Shebekino, Belgorod-regionen”
Funktioner för att lösa och utvärdera uppgifter 30-35 i Unified State Exam i kemi
Förberedd av: Arnautova Natalya Zakharovna,
lärare i kemi och biologi
MBOU "Secondary school No. 4, Shebekino, Belgorod region"
2017
Metodik för att bedöma uppgifter med ett detaljerat svar (huvudsakliga metoder för att fastställa kriterier och betygsskalor för att slutföra uppgifter)
Grunden för metodiken för att bedöma uppgifter med utförligt svar är ett antal allmänna bestämmelser. De viktigaste bland dem är följande:
Testning och utvärdering av uppgifter med utförligt svar utförs endast genom en oberoende granskning baserad på metoden moment för momentanalys av examinandens svar.
Användningen av analysmetoden element för element gör det nödvändigt att säkerställa att ordalydelsen av uppgiftsvillkoren tydligt överensstämmer med de innehållselement som kontrolleras. Listan över innehållselement som testas av alla uppdrag överensstämmer med standardkraven för förberedelsenivån för gymnasieutexaminerade.
Kriteriet för att bedöma slutförandet av en uppgift med hjälp av metoden för element-för-element-analys är att fastställa närvaron av de givna svarselementens svar i examinatorernas svar
i svarsmodellen. En annan svarsmodell som föreslagits av examinanden kan dock accepteras om den inte förvränger essensen av den kemiska komponenten i uppgiftsvillkoren.
Betygsskalan för uppgiftsutförande fastställs beroende på antalet innehållselement som ingår i svarsmodellen och med hänsyn till sådana faktorer som:
Nivå av komplexitet för innehållet som testas;
En specifik sekvens av åtgärder som bör utföras när en uppgift utförs;
Entydig tolkning av uppgiftens förutsättningar och möjliga alternativ för att formulera svaret;
Uppfyllelse av uppdragsvillkoren med de föreslagna bedömningskriterierna för enskilda innehållselement;
Ungefär samma svårighetsgrad för vart och ett av innehållselementen som testas av uppgiften.
Vid utveckling av bedömningskriterier beaktas egenskaperna hos innehållsdelarna i alla fem långsvarsuppgifter som ingår i tentamensuppgiften. Det tas också hänsyn till att protokollen över examinandens svar kan vara antingen mycket generella, strömlinjeformade och inte specifika eller för korta.
och otillräckligt motiverad. Stor uppmärksamhet ägnas åt att lyfta fram de delar av svaret som är värda en poäng. Detta tar hänsyn till det oundvikliga i en gradvis ökning av svårigheten att få varje efterföljande poäng
för ett korrekt formulerat innehållselement.
När man upprättar en skala för att betygsätta beräkningsproblem (33 och 34) beaktas möjligheten till olika sätt att lösa dem, och därför förekomsten i examinandens svar av huvudstadierna och resultaten av att utföra de angivna uppgifterna.
i utvärderingskriterierna. Låt oss illustrera metodiken för att bedöma uppgifter med ett detaljerat svar med hjälp av specifika exempel.
läsåret 2017-2018
UppdragMaxpoäng
Jobbnivå
Uppgift 30
2016-2017
Uppgifterna 30 syftar till att testa förmågan att bestämma graden av oxidation kemiska grundämnen, bestämma oxidationsmedlet och reduktionsmedlet, förutsäga produkterna från redoxreaktioner, fastställa formlerna för ämnen som saknas i reaktionsschemat, upprätta en elektronisk balans och på basis av den tilldela koefficienter i reaktionsekvationer.
Skalan för att bedöma utförandet av sådana uppgifter inkluderar följande delar:
ett elektroniskt saldo har sammanställts – 1 poäng;
oxidationsmedlet och reduktionsmedlet anges – 1 poäng.
Formler för saknade ämnen bestäms och koefficienter tilldelas
i redoxreaktionens ekvation – 1 poäng.
Exempel på uppgift:
Använd elektronbalansmetoden och skapa en ekvation för reaktionen
Na 2 SO 3 + … + KOH K 2 MnO 4 + … + H 2 O
Identifiera oxidationsmedlet och reduktionsmedlet.
Poäng
Svarsalternativ
Mn +7 + ē → Mn +6
S +4 – 2ē → S +6
Svavel i +4-oxidationstillståndet (eller natriumsulfit på grund av svavel i +4-oxidationstillståndet) är ett reduktionsmedel.
Mangan i oxidationstillstånd +7 (eller kaliumpermanganat på grund av mangan
i oxidationstillstånd +7) – oxidationsmedel.
Na2SO3 + 2KMnO4 + 2KOH = Na2SO4 + 2K2MnO4 + H2O
Svaret är korrekt och komplett:
graden av oxidation av element som är ett oxidationsmedel respektive ett reduktionsmedel i reaktionen bestäms;
oxidations- och reduktionsprocesser registrerades, och en elektronisk (elektron-jon) balans sammanställdes på grundval av dessa;
de saknade ämnena i reaktionsekvationen bestäms, alla koefficienter placeras
Maxpoäng
Vid bedömning av examinandens svar är det nödvändigt att ta hänsyn till att det inte finns några enhetliga krav på formateringen av svaret på denna uppgift. Som ett resultat accepteras sammanställningen av både elektroniska balanser och elektronjonbalanser som det korrekta svaret, och indikeringen av oxidationsmedel och reduktionsmedel kan göras på vilket som helst klart begripligt sätt. Men om svaret innehåller delar av svaret som är ömsesidigt uteslutande i betydelse, kan de inte anses vara korrekta.
2018 format uppgifter
1. Uppgift 30 (2 poäng)
För att slutföra uppgiften, använd följande listaämnen: kaliumpermanganat, väteklorid, natriumklorid, natriumkarbonat, kaliumklorid. Det är tillåtet att använda vattenlösningar av ämnen.
Från den föreslagna listan över ämnen, välj ämnen mellan vilka en oxidations-reduktionsreaktion är möjlig och skriv ner ekvationen för denna reaktion. Gör en elektronisk våg, ange oxidationsmedel och reduktionsmedel.
Förklaring.
Låt oss skriva reaktionsekvationen:
Låt oss skapa ett elektroniskt saldo:

Klor i oxidationstillstånd −1 är ett reduktionsmedel. Mangan i oxidationstillståndet +7 är ett oxidationsmedel.TOTALT 2 poäng
ämnen väljs, redoxreaktionens ekvation skrivs och alla koefficienter ställs in.
oxidations- och reduktionsprocesser registrerades och en elektronisk (elektron-jon) balans sammanställdes på grundval av dessa; vilka är oxidationsmedlet respektive reduktionsmedlet i reaktionen;
Det uppstod ett fel i endast ett av svarselementen ovan
Det fanns fel i två av ovanstående svarselement
Alla delar av svaret är felaktigt skrivna
Maxpoäng
2018 format uppgifter
1. Uppgift 31 (2 poäng)
För att slutföra uppgiften, använd följande lista över ämnen: kaliumpermanganat, kaliumbikarbonat, natriumsulfit, bariumsulfat, kaliumhydroxid. Det är tillåtet att använda vattenlösningar av ämnen.
Förklaring.
Möjligt svar:
2. Uppgift 31
För att slutföra uppgiften, använd följande lista med ämnen: väteklorid, silver(I)nitrat, kaliumpermanganat, vatten, salpetersyra. Det är tillåtet att använda vattenlösningar av ämnen.
Från den föreslagna listan över ämnen, välj ämnen mellan vilka en jonbytesreaktion är möjlig. Skriv ner de molekylära, fullständiga och förkortade jonekvationerna för denna reaktion.
Förklaring.
Möjligt svar:
Uppgift 32. 2018 format uppgifter
I tillståndet av uppgift 32, testande av kunskap om det genetiska förhållandet mellan olika klasser av oorganiska ämnen, föreslås en beskrivning av ett specifikt kemiskt experiment, vars framsteg examinatorerna måste illustrera med hjälp av ekvationerna för motsvarande kemiska reaktioner. Betygsskalan för uppgiften är densamma som 2016, lika med 4 poäng: varje korrekt skriven reaktionsekvation får 1 poäng.
Exempel på uppgift:
Järn löstes i varm koncentrerad svavelsyra. Det resulterande saltet behandlades med ett överskott av natriumhydroxidlösning. Den bruna fällningen som bildades filtrerades och kalcinerades. Den resulterande substansen upphettades med järn.
Skriv ekvationer för de fyra beskrivna reaktionerna.
Innehåll i rätt svar och bedömningsanvisningar(annan formulering av svaret är tillåten som inte förvränger dess innebörd)Poäng
Svarsalternativ
Fyra ekvationer för de beskrivna reaktionerna skrivs:
1) 2Fe + 6H2SO4  Fe2(SO4)3 + 3SO2 + 6H2O
Fe2(SO4)3 + 3SO2 + 6H2O
2) Fe2 (SO4)3 + 6NaOH = 2Fe(OH)3 + 3Na2SO4
3) 2Fe(OH) 3  Fe2O3 + 3H2O
Fe2O3 + 3H2O
4) Fe2O3 + Fe = 3FeO
Alla reaktionsekvationer är felaktigt skrivna
Maxpoäng
Det bör noteras att frånvaron av koefficienter (minst en) före formlerna för ämnen i reaktionsekvationer anses vara ett fel. Inga poäng ges för en sådan ekvation.
Uppgift 33. 2018 format uppgifter
Uppgifter 33 testar assimileringen av kunskap om förhållandet mellan organiska ämnen och ger möjlighet att kontrollera fem innehållselement: riktigheten av att skriva fem reaktionsekvationer som motsvarar diagrammet - en "kedja" av transformationer. Vid skrivning av reaktionsekvationer ska examinander använda organiska ämnens strukturformler. Närvaron av varje markerat innehållselement i svaret får 1 poäng. Det maximala antalet poäng för att utföra sådana uppgifter är 5.
Exempel på uppgift:
Skriv reaktionsekvationerna som kan användas för att utföra följande transformationer:

När du skriver reaktionsekvationer, använd strukturformlerna för organiska ämnen.
Innehåll i rätt svar och bedömningsanvisningarAndra formuleringar av svaret är tillåtna som inte förvränger dess innebörd)
Poäng
Svarsalternativ
Fem reaktionsekvationer har skrivits motsvarande transformationsschemat:


Fem reaktionsekvationer skrivna korrekt
Fyra reaktionsekvationer skrivna korrekt
Tre reaktionsekvationer skrivna korrekt
Två reaktionsekvationer skrivna korrekt
En reaktionsekvation skriven korrekt
Alla delar av svaret är felaktigt skrivna
Maxpoäng
Observera att det i examinandens svar är tillåtet att använda strukturformler olika typer(expanderat, sammandraget, skelett), vilket otvetydigt återspeglar atomernas bindningsordning och det relativa arrangemanget av substituenter och funktionella grupper
i en molekyl av organiskt material.
Uppgift 34. 2018 format uppgifter
Uppgifter 34 är beräkningsproblem. Deras genomförande kräver kunskap kemiska egenskaperämnen och innebär genomförande av en viss uppsättning åtgärder för att säkerställa att rätt svar erhålls. Bland sådana åtgärder nämner vi följande:
– utarbeta ekvationer av kemiska reaktioner (enligt data om problemförhållandena) som är nödvändiga för att utföra stökiometriska beräkningar;
– utföra beräkningar som krävs för att hitta svar på frågor
i problemformuleringen finns frågor;
– formulera ett logiskt underbyggt svar på alla frågor som ställs i uppgiftsvillkoren (till exempel fastställande av en molekylformel).
Man bör dock komma ihåg att inte alla de namngivna åtgärderna nödvändigtvis måste vara närvarande när man löser ett beräkningsproblem, och i vissa fall kan vissa av dem användas mer än en gång.
Maxpoängen för att slutföra uppgiften är 4 poäng. När du kontrollerar bör du först och främst vara uppmärksam på den logiska giltigheten av de utförda åtgärderna, eftersom vissa uppgifter kan lösas på flera sätt. Samtidigt, för att objektivt utvärdera den föreslagna metoden för att lösa problemet, är det nödvändigt att kontrollera riktigheten av de mellanliggande resultaten som användes för att få svaret.
Exempel på uppgift:
Bestäm massfraktionerna (i%) av järn(II)sulfat och aluminiumsulfid
i en blandning om, när 25 g av denna blandning behandlas med vatten, en gas frigörs som fullständigt reagerar med 960 g av en 5% lösning av kopparsulfat.
I ditt svar, skriv ner reaktionsekvationerna som anges i problemformuleringen,
och tillhandahåll alla nödvändiga beräkningar (ange måttenheterna för de erforderliga fysiska storheterna).
Svarsalternativ
Reaktionsekvationerna sammanställdes:
Mängden svavelväte beräknas:
Mängden ämne och massa av aluminiumsulfid och järn(II)sulfat beräknas:

Massfraktionerna av järn(II)sulfat och aluminiumsulfid i den initiala blandningen bestämdes:
ω(FeSO4) = 10/25 = 0,4 eller 40 %
ω(Al2S3) = 15/25 = 0,6 eller 6 0 %
Svaret är korrekt och komplett:
svaret innehåller korrekt reaktionsekvationer som motsvarar villkoren för uppgiften;
beräkningar har utförts korrekt med hjälp av de nödvändiga fysiska kvantiteterna som anges i arbetsvillkoren;
ett logiskt underbyggt samband mellan de fysiska storheter på grundval av vilka beräkningar utförs visas;
i enlighet med arbetsvillkoren bestäms den erforderliga fysiska kvantiteten
Det uppstod ett fel i endast ett av svarselementen ovan
Alla delar av svaret är felaktigt skrivna
Maxpoäng
Vid kontroll av svaret ska examinanden ta hänsyn till att om svaret innehåller ett beräkningsfel i något av de tre momenten (andra, tredje eller fjärde), vilket ledde till ett felaktigt svar, är betyget för att ha slutfört uppgiften. minskat med endast 1 poäng.
Uppgift 35. 2018 format uppgifter
Uppgifter 35 innebär att bestämma molekylformeln för ett ämne. Att slutföra denna uppgift inkluderar följande sekventiella operationer: utföra de beräkningar som är nödvändiga för att fastställa molekylformeln för ett organiskt ämne, skriva molekylformeln för ett organiskt ämne, utarbeta en strukturformel för ett ämne som unikt återspeglar ordningen för atombindningar i sin molekyl, skriver en reaktionsekvation som uppfyller villkoren för uppgiften.
Betygsskalan för uppgift 35 i del 2 av tentamensuppgiften blir 3 poäng.
Uppgifter 35 använder en kombination av testade innehållselement - beräkningar, på grundval av vilka de kommer att bestämma molekylformeln för ett ämne, sammanställa en allmän formel för ett ämne och sedan bestämma molekyl- och strukturformeln för ett ämne på grundval av dess .
Alla dessa åtgärder kan utföras i olika sekvenser. Examinanden kan med andra ord komma fram till svaret på vilket logiskt sätt som helst som är tillgängligt för honom. Därför, när man bedömer en uppgift, ägnas den största uppmärksamheten åt riktigheten av den valda metoden för att bestämma molekylformeln för ett ämne.
Exempel på uppgift:
När ett prov av någon organisk förening som väger 14,8 g bränns, erhålls 35,2 g koldioxid och 18,0 g vatten.
Det är känt att den relativa ångdensiteten för detta ämne med avseende på väte är 37. Under studiet av de kemiska egenskaperna hos detta ämne konstaterades att när detta ämne interagerar med koppar(II)oxid bildas en keton.
Baserat på uppgifterna för uppgiftsvillkoren:
1) gör de beräkningar som krävs för att fastställa molekylformeln för ett organiskt ämne (ange måttenheterna för de erforderliga fysikaliska kvantiteterna);
skriv ner molekylformeln för det ursprungliga organiska ämnet;
2) utarbeta en strukturformel för detta ämne, som otvetydigt återspeglar ordningen för bindningar av atomer i dess molekyl;
3) skriv ekvationen för reaktionen av detta ämne med koppar(II)oxid med hjälp av ämnets strukturformel.
Innehåll i rätt svar och bedömningsanvisningar(annan formulering av svaret är tillåten som inte förvränger dess innebörd)
Poäng
Svarsalternativ
Mängden av förbränningsproduktsubstans som hittades:
Den allmänna formeln för ämnet är C x H y O z
n(CO2) = 35,2/44 = 0,8 mol; n(C) = 0,8 mol
n(H2O) = 18,0/18 = 1,0 mol; n(H) = 1,0 ∙ 2 = 2,0 mol
m(O) = 14,8 – 0,8 ∙ 12 – 2 = 3,2 g; n(O) = 3,2 ⁄ 16 = 0,2 mol
Ämnets molekylformel bestämdes:
x:y:z = 0,8:2:0,2 = 4:10:1
Den enklaste formeln är C 4 H 10 O
M enkel (C4H10O) = 74 g/mol
M-källa (C x H y Oz) = 37 ∙ 2 = 74 g/mol
Molekylformel för utgångsämnet – C 4 H 10 O
Ämnets strukturformel har sammanställts:

Ekvationen för reaktionen mellan ett ämne och koppar(II)oxid är skrivet:
Svaret är korrekt och komplett:
de beräkningar som krävs för att fastställa molekylformeln för ett ämne har utförts korrekt; ämnets molekylformel skrivs ner;
den organiska substansens strukturformel skrivs ner, vilket återspeglar bindningsordningen och det relativa arrangemanget av substituenter och funktionella grupper i molekylen i enlighet med tilldelningsvillkoren;
reaktionsekvationen, som anges i uppgiftsvillkoren, skrivs med hjälp av strukturformeln för ett organiskt ämne
Det uppstod ett fel i endast ett av svarselementen ovan
Det fanns fel i två av ovanstående svarselement
Det fanns fel i tre av ovanstående svarselement
Alla delar av svaret är felaktigt skrivna
Alla delar av svaret är felaktigt skrivna
Maxpoäng
TOTAL del 2
2+2+ 4+5+4 +3=20 poäng
Referenser
1. Metodiskt material för ordförande och ledamöter av ämneskommissioner för de konstituerande enheterna i Ryska federationen att kontrollera slutförandet av uppgifter med ett detaljerat undersökningssvar Unified State Examination fungerar 2017. Artikel "Metodologiska rekommendationer för bedömning av utförandet av Unified State Examination-uppgifter med en detaljerad fråga." Moskva, 2017.
2. FIPI-projekt för att testa och mäta material för Unified State Exam 2018.
3. Demoversioner, specifikationer, kodifierare av Unified State Exam 2018. FIPI hemsida.
4. Information om planerade ändringar av 2018 års CMM. FIPI hemsida.
5. Webbplatsen "Jag kommer att lösa Unified State Exam": kemi, för en expert.
Ett av de valbara ämnen som en gymnasieutbildad anger i ansökan är Unified State Exam in Chemistry 2018. Provmaterial i kemi utarbetas enl. Federal standard fullfölja gymnasieutbildning. De är helt inriktade på skolnivå. Svårigheten är att det i gymnasieskolorna endast avsätts en timme i veckan för studier i kemi. Därför, för att klara Unified State Examen i kemi, måste du förbereda dig ihärdigt och målmedvetet.
Vem väljer kemi för Unified State Exam?
Unified State Exam in Chemistry väljs av elever i årskurs 11 som planerar att ytterligare koppla ihop sina liv med studier vid högre utbildningsinstitutioner inom detta ämnesområde.
- Som regel är dessa akademiker som vill komma in på tekniska universitet som erbjuder kemiska specialiteter som en utbildningsprofil.
- Det kan också vara killar som vill skriva in sig på medicinska universitet, där goda kunskaper i kemi krävs.
Grundläggande dokument för Unified State Exam
Om vi pratar om innehållet i examensprovet i kemi, måste du här bekanta dig med tre huvuddokument:
1)Kodifierare, bestående av två delar.
- Den första delen av dokumentet presenterar de delar av innehållet som alla uppgifter som ingår i alternativet syftar till att kontrollera att de är fullständiga.
- Den andra delen av kodifieraren kallas "Lista över krav för utbildningsnivån för utexaminerade." Här är en lista över färdigheter som en elev i 11:e klass måste behärska för att klara uppgifterna.
2) Specifikation. Detta är ett dokument som reglerar strukturen för innevarande års Unified State Examination. Den presenterar ämnen som kan förekomma på provet.
3) Demoversion av Unified State Exam in Chemistry- det här är en version av Unified State Exam, som du måste börja förbereda dig för statlig examen i kemi.
Hur förbereder man sig? Vad ska man läsa?
Det finns ett ganska stort antal manualer som är hjälpmaterial:
- De böcker som rekommenderas av utbildningsministeriet är läroböcker i kemi.
- Förmåner märkta "FIPI".
- Böcker av utvecklarna av Unified State Exam KIMs själva i kemi.
Hur fungerar Unified State Exam?
| Totalt 34 uppgifter | |
| Del 1 | del 2 |
| 29 korta svarsfrågor | 5 uppgifter med detaljerade svar |
Tiden för att genomföra hela tentamen är 210 minuter (3 timmar 30 minuter).
Maximal primärpoäng – 60.
Del 1 presenterar uppgifter för grundläggande och högre nivå komplexitet.
Del 2 innehåller uppgifter på hög nivå.
Struktur och typologi av uppgifter i 1:a delen av KIM
Del 1-uppgifter finns i två huvudsakliga former:
- kortsvarsuppgifter som involverar upprättande av korrespondens mellan positionerna i två uppsättningar;
- välja flera svarsalternativ från listan.
Till exempel i den första uppgiften grundläggande nivå ett antal kemiska grundämnen kan anges (5 grundämnen totalt). Därefter ställs frågor som den utexaminerade måste läsa noggrant och ge lämpligt svar. Det faktum att det finns två celler i svarsfältet indikerar att det bör finnas två sådana svar. Och bara genom att välja alla svarsalternativ korrekt kan du få maximal poäng för denna uppgift.
Det andra exemplet på uppgifter är uppgifter om korrespondens mellan två uppsättningar (5:e uppgiften). Således kan formler för ämnen presenteras i den vänstra kolumnen och i den högra kolumnen - klassen (gruppen) av ämnen som detta eller det ämnet tillhör. Eftersom det finns 3 ämnen i den vänstra kolumnen måste eleven upprätta 3 motsvarigheter.
Om vi talar om uppgifter av en annan typ, då kan vi se uppgifter som innehåller textinformation i större utsträckning, där någon form av mental uppförande av ett kemiskt experiment antas och valet av formler för ämnen som gör att du kan svara korrekt på uppgift som presenteras i uppgiftsvillkoren.
Flervalsuppgifter verkar ofta ganska enkla för eleverna och kräver inte att man skriver ner reaktionsekvationer eller formler för ämnen. Tyvärr är så inte fallet. Bara om den utexaminerade faktiskt föreskriver en lösning för varje uppgift och är eftertänksam detta tillstånd problem, då finns det i det här fallet en sannolikhet att komma fram till rätt svar.
Funktioner av uppgifterna i den andra delen

Men uppgifterna från den andra delen av testet med ett utförligt svar tyder på en högre svårighetsgrad. Men detta går inte utöver de ämnen som presenteras i kodifieraren. Komplikationen beror på det faktum att om testet i uppgifter på en grundläggande nivå är inriktat på ett innehållselement, så förutsätts i uppgifter med hög komplexitet behärskning av flera innehållselement eller flera färdigheter. Till exempel behöver du inte bara klassificera ett visst ämne i en klass eller grupp av ämnen, utan också komma ihåg vilka egenskaper denna grupp av ämnen har ibland måste du komma ihåg de specifika egenskaperna hos de ämnen som diskuteras i uppgiften.
Fem uppgifter med utförliga svar riktar sig till de viktigaste, viktigaste avsnitten i kemikursen. Hela alternativet kan delas in i vissa innehållsblock, av vilka många är förstorade ämnen i skolans kemikurs. Till exempel "Atomens struktur", "Periodiska lagar. Periodiska systemet för kemiska grundämnen”, ”Oorganiska ämnen”, ”Organiska ämnen”, ”Kunskapsmetoder i kemi”, ”Kemi i livet”, ”Beräkningar enl. kemiska formler, reaktionsekvationer".
Vad kan du använda under provet?
Kandidaten måste ta med två saker till kemiprovet:
- icke-programmerbar miniräknare;
- svart gelpenna.
Provet ger dig:
- periodiskt system av kemiska grundämnen av D. I. Mendeleev;
- Tabell över lösligheten av syror, salter och baser;
- elektrokemiska spänningsserier av metaller (metallaktivitetsserier).
Utbildningsministeriet avser inte att göra några ändringar i Unified State Exam KIM i kemi 2017–2018 läsår.
Datumet för Unified State Examination i kemi kommer att bli känt i januari 2018.
OM Unified State Exam resultat i kemi 2018 kan hittas på din skola eller på den officiella webbplatsen för Unified State Exam.
För mer information om funktionerna i Unified State Exam i kemi, titta på videon:
Tabell 1
Det maximala antalet poäng som en examinand kan få för att fullfölja hela OGE tentamen i kemi (utan ett riktigt experiment) är 34 poäng.
Provresultaten kan användas vid antagning av elever till specialklasser i gymnasieskolor. Riktlinjen för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 23 poäng.
Skala för att omvandla den primära poängen för att slutföra en tentamen till ett betyg på en femgradig skala (att arbeta med ett riktigt experiment, demoversion 2)
Tabell 2
En riktlinje för urval till specialiserade klasser kan vara en indikator vars nedre gräns motsvarar 25 poäng.
Det maximala antalet poäng som en examinand kan få för att fullfölja hela tentamensuppsatsen (med ett riktigt experiment) är 38 poäng.
Ett system för att bedöma slutförandet av individuella uppgifter och OGE 2018 tentamen i kemi som helhet.
Elevernas svar på uppgifter i del 1 kontrolleras av experter eller med hjälp av en dator. Korrekt slutförande av var och en av uppgifterna 1–15 får 1 poäng. Rätt genomförd var och en av uppgifterna 16–19 bedöms med max 2 poäng.
Uppgift 16 och 17 anses vara korrekt genomförda om två svarsalternativ är korrekt valda i var och en av dem. För ett ofullständigt svar - ett av två svar är korrekt namngivet eller tre svar är namngivna, varav två är rätt - ges 1 poäng. De återstående svarsalternativen övervägs otrogen och får 0 poäng.
Uppgifterna 18 och 19 anses vara korrekt genomförda om tre överensstämmelser är korrekt upprättade. Ett svar där två av tre matchningar fastställs anses vara delvis korrekt; det är värt 1 poäng. De återstående alternativen anses vara ett felaktigt svar och får 0 poäng.
Uppgifterna i del 2 (20–23) kontrolleras av en ämneskommission. När experten bedömer var och en av de tre uppgifterna, identifierar experten, baserat på att jämföra kandidatens svar med provsvaret i bedömningskriterierna, element i studentens svar, som var och en är värd 1 poäng. Maxpoäng för en korrekt utförd uppgift: för uppgifter 20 och 21 - 3 poäng vardera; i modell 1 för uppgift 22 – 5 poäng; i modell 2 för uppgift 22 - 4 poäng, för uppgift 23 - 5 poäng.
Uppgifter med ett utförligt svar kan eleverna utföra på olika sätt. Därför bör de exempellösningar som ges i utvärderingskriterierna endast betraktas som ett av de möjliga svarsalternativen. Det gäller i första hand metoder för att lösa beräkningsproblem.
Att klara slutprov i skolan. Det kommer att behöva tas för antagning till universitet inom följande områden: kemi och kemisk teknik, medicin, konstruktion, bioteknik och andra. I allmänhet är provet inte särskilt populärt - bara en student av tio utexaminerade väljer kemi.
Checka ut allmän information om provet och börja förbereda. KIM-versionen av Unified State Exam 2019 har vissa skillnader från förra året: 1) i del 2 lades en uppgift med hög svårighetsgrad med ett detaljerat svar till, 2) för fyra frågor svårighetsgraden och högsta primärpoäng reviderades (för hela testet ändrades inte maximalpoängen), 3) för För att säkerställa en tydligare fördelning av uppgifter i tematiska block ändrade utvecklarna sin ordning något i del 1.
Unified State Examination
Förra året, för att klara Unified State Examination i kemi med minst ett C, räckte det för att få 37 primärpoäng. De gavs till exempel för att ha utfört de första 15 uppgifterna i testet korrekt.
Det är ännu inte känt exakt vad som kommer att hända under 2019: vi måste vänta på den officiella ordern från Rosobrnadzor om korrespondensen mellan primära och testresultat. Troligtvis dyker den upp i december. Med tanke på att den maximala primära poängen för hela testet förblir densamma, kommer sannolikt inte heller minimipoängen att ändras. Låt oss fokusera på dessa tabeller för tillfället:
Struktur för Unified State Exam-testet
Under 2019 består testet av två delar, inklusive 35 uppgifter.
- Del 1: 29 uppgifter (1–29) med ett kort svar (nummer eller talföljd);
- Del 2: 6 uppgifter (30–36) med utförliga svar, kompletta lösningar på uppgifterna skrivs ner på svarsblad 2.
Förberedelse för Unified State Exam
- Gör Unified State Exam-testen online gratis utan registrering eller SMS. Proven som presenteras är identiska i komplexitet och struktur med de faktiska proven som genomförts under motsvarande år.
- Ladda ner demoversioner av Unified State Examination in Chemistry, vilket gör att du bättre kan förbereda dig för provet och klara det lättare. Alla föreslagna tester har utvecklats och godkänts för förberedelser för Unified State Exam av Federal Institute of Pedagogical Measurements (FIPI). I samma FIPI alla officiella Alternativ för Unified State Exam.
De uppgifter som du kommer att se kommer med största sannolikhet inte att visas på tentamen, utan kommer att likna demo, om samma ämne eller helt enkelt med olika nummer. - Bekanta dig med de grundläggande formlerna för provförberedelser för att fräscha upp ditt minne innan du provar demos och testalternativen.
Allmänna siffror för Unified State Examination
| År | Minimum Unified State Examination poäng | Genomsnittlig poäng | Antal deltagare | Misslyckades, % | Antal 100 poäng |
Varaktighet- Tentamens längd, min. |
| 2009 | 33 | |||||
| 2010 | 33 | 56,04 | 83 544 | 6,2 | 275 | 180 |
| 2011 | 32 | 57,75 | 77 806 | 8,6 | 331 | 160 |
| 2012 | 36 | 57,3 | 93 181 | 11 | 365 | 180 |
| 2013 | 36 | 67,8 | 93 802 | 7,3 | 3220 | 180 |
| 2014 | 36 | 55,3 | 180 | |||
| 2015 | 36 | 56,3 | 180 | |||
| 2016 | 36 | 180 | ||||
| 2017 | 36 | 180 | ||||
| 2018 |